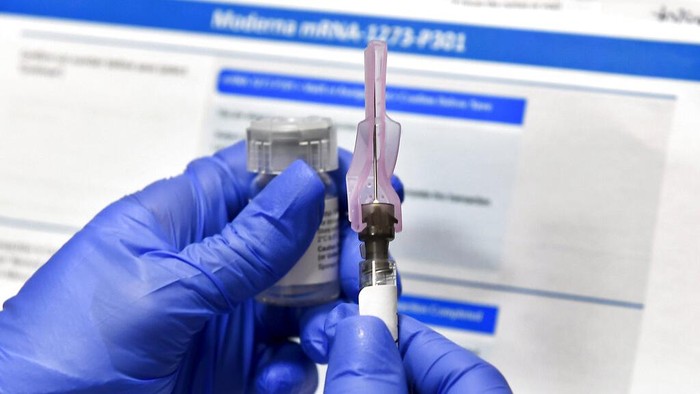
Pejabat kesehatan Inggris mewanti-wanti soal vaksin Corona Pfizer-BioNTech yang bisa menimbulkan reaksi alergi. Peringatan ini juga menjadi pertimbangan Amerika Serikat (AS) ketika memakai vaksin Pfizer-BioNTech.
Dilansir AFP, Kamis (10/12/2020) peringatan itu muncul setelah dua anggota Layanan Kesehatan Nasional yang dikelola negara, yang termasuk di antara yang pertama menerima vaksin itu pada Selasa (8/12), mengalami reaksi alergi dan membutuhkan perawatan.
Direktur medis NHS Inggris, Stephen Powis mengatakan bahwa kedua orang tersebut, yang memiliki riwayat reaksi alergi, sekarang pulih dengan baik.
Powis mengatakan bahwa Badan Pengatur Obat dan Produk Kesehatan independen (MHRA) sekarang telah menyarankan bahwa "orang dengan riwayat reaksi alergi yang signifikan tidak boleh menerima vaksinasi ini" sebagai tindakan pencegahan.
Reaksi alergi "signifikan" termasuk terhadap obat-obatan, makanan atau vaksin, menurut MHRA.
Ribuan warga Inggris menjadi yang pertama di dunia Barat yang menerima vaksin COVID-19 yang disetujui pada hari Selasa (8/12), ketika NHS memulai upaya vaksinasi terbesar sejak dibuat pada tahun 1948.
Vaksin ini diberikan dalam dua dosis, dengan jarak 21 hari. Orang-orang yang berusia di atas 80-an tahun serta staf perawatan kesehatan dan sosial berada di urutan pertama yang mendapatkan vaksin ini.
Inggris telah menerima sekitar 800.000 dosis vaksin dalam gelombang pertama dari pesanan 40 juta dosis vaksin. Hingga empat juta dosis diharapkan tersedia pada akhir Desember ini.
Kepala eksekutif Pfizer, Albert Bourla pada hari Selasa (8/12) mengatakan dia memahami kekhawatiran global tentang kecepatan perusahaan farmasi dalam memproduksi vaksin untuk melawan COVID-19.
Namun dia bersikeras tidak ada jalan pintas yang dipotong.
Vaksin itu telah diuji "dengan cara yang persis sama seperti kami menguji vaksin apa pun yang beredar di luar sana", katanya dalam pengarahan media virtual di Jenewa, Swiss.
Pfizer mengatakan MHRA telah memberitahukannya tentang reaksi alergi tetapi mengatakan selama uji coba fase 3 terhadap lebih dari 40.000 orang, hasilnya baik. "Vaksin itu umumnya ditoleransi dengan baik tanpa masalah keamanan yang serius," ujarnya.
Bagaimana tanggapan AS soal peringatan ini? Silakan klik halaman selanjutnya.
Sementara itu, Badan Pengawas Obat dan Makanan Amerika Serikat (FDA) belum menyetujui untuk memesan vaksin Pfizer-BioNTech COVID-19. Namun, FDA mungkin akan meminta orang-orang dengan riwayat reaksi alergi parah untuk tidak divaksinasi dengan vaksin ini.
Dilansir AFP, Kamis (10/12/2020) berita itu menyusul peringatan di Inggris.
Moncef Slaoui, yang merupakan penasihat utama program AS untuk pengembangan vaksin dan pengobatan COVID-19, mengatakan bahwa pihaknya melihat data.
"Melihat data, pasien atau subjek dengan riwayat reaksi alergi parah telah dikeluarkan dari uji klinis," kata Slaoui.
"Saya berasumsi - karena FDA akan membuat keputusan tersebut - bahwa besok ini akan menjadi bagian dari pertimbangan, dan seperti di Inggris, harapannya adalah subjek dengan reaksi parah yang diketahui, (akan diminta) untuk tidak mengambil vaksin, sampai kami memahami dengan tepat apa yang terjadi di sini," tuturnya.
FDA mungkin juga akan meminta penyedia untuk mengawasi apakah orang-orang mengalami bentuk kelumpuhan wajah yang langka, meski sementara dan tidak terlalu serius yang disebut Bell's palsy. Pasalnya, data menunjukkan empat orang dari sekitar 19.000 orang dalam kelompok uji coba vaksin mengalami kondisi tersebut.
Secara keseluruhan, Slaoui mengatakan dia terkesan dengan data vaksin yang muncul dalam dokumen pengarahan yang diserahkan ke FDA, termasuk yang penting bahwa perlindungan yang kuat dimulai setelah dosis pertama - meskipun rekomendasinya tetap untuk mengambil suntikan vaksin kedua, dengan selisih 21 hari.